5月21日,中国科学院武汉病毒研究所/生物安全大科学研究中心成功开发新型冠状病毒SARS-CoV-2转基因小鼠模型,以“Pathogenesis of SARS-CoV-2 in transgenic mice expressing human angiotensin-converting enzyme2”为题在线发表(论文链接附后)。研究团队使用SARS-CoV-2感染HFH4-hACE2小鼠(使用HFH4肺纤毛上皮细胞特异性启动子将hACE2基因转入小鼠中),通过持续监测小鼠临床症状,观察组织病理变化以及各组织中病毒载量情况,发现感染的小鼠产生了与COVID-19患者类似的间质性肺炎;预先暴露于SARS-CoV-2可以保护小鼠免受病毒的致死感染。该模型的建立为测试潜在疫苗和抗病毒药物提供了有利的工具。
研究团队前期鉴定出SARS-CoV-2利用人血管紧张素转化酶2(hACE2)作为受体入侵宿主细胞而无法使用鼠血管紧张素转化酶2(mACE2),这意味着普通小鼠可能无法有效感染SARS-CoV-2。为了建立SARS-CoV-2小动物感染模型,研究团队迅速利用优势资源,使用实验室之前引进的HFH4-hACE2转基因小鼠对SARS-CoV-2的致病性进行研究。作者在使用SARS-CoV-2感染小鼠后,发现部分小鼠出现明显的体重降低并最终死亡。小鼠肺部在感染第1天和第3天时就出现少量炎性细胞浸润和纤维蛋白渗出的情况。从感染后5天起,小鼠出现重症和轻症两种不同的表型:重症小鼠(27.3%)肺部展现出严重的血管周-支气管周炎性细胞浸润,伴有部分支气管堵塞和透明膜形成;轻症小鼠肺部炎症反应减轻并逐渐恢复正常。病毒载量结果显示SARS-CoV-2主要感染小鼠的肺组织,但在部分小鼠的眼睛,心脏和脑组织中也发现了病毒RNA。
研究团队同时观察了SARS-CoV-2感染小鼠的生存率情况,发现部分小鼠在感染后死亡,主要原因可能是hACE2在小鼠脑中表达所致。通过对感染存活小鼠和未感染过的小鼠进行高剂量攻毒,发现被感染过的小鼠可以免受病毒的致死性攻击(图1)。
这项研究发现HFH4-hACE2转基因小鼠模型对SARS-CoV-2易感,小鼠肺组织是病毒的主要靶器官并且能部分模拟COVID-19的病理变化;预先暴露于病毒能保护小鼠免受严重的肺部感染(图2)。该模vv型的成功建立给疫苗及抗病毒药物提供了简便,高效的测试平台,为新冠肺炎疫情的控制提供了有力的科技支撑。
武汉病毒研究所博士研究生蒋人地、刘美琴、陈颖为该论文的共同第一作者,石正丽研究员与杨兴娄副研究员为该论文的共同通讯作者。北卡罗莱纳大学教堂山分校Ralph Baric教授为该论文的合作者。这项工作得到中科院先导专项、国家自然科学基金、中科院青促会等项目的大力支持。
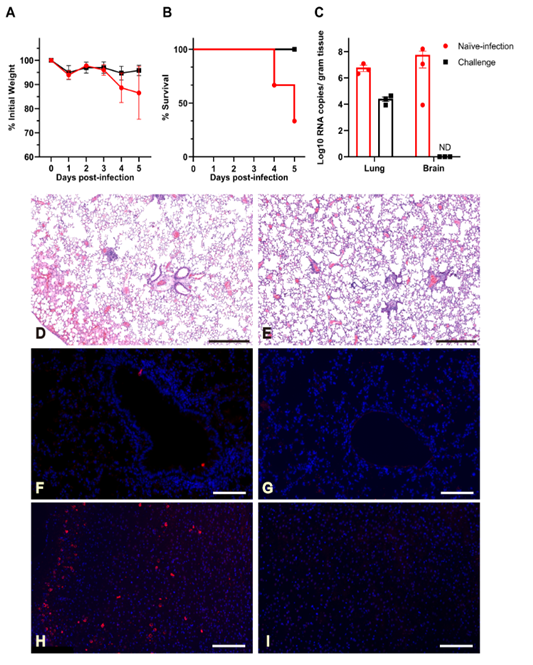
图1.预先暴露于SARS-CoV-2可保护小鼠免受严重肺部感染。存活小鼠及初次感染小鼠在高剂量SARS-CoV-2感染后的体重变化情况(A);生存率情况(B);主要器官病毒载量情况(C);肺组织病理变化及肺组织与脑组织病毒抗原表达情况:初次感染(D,F,H),再次感染(E,G,I)。
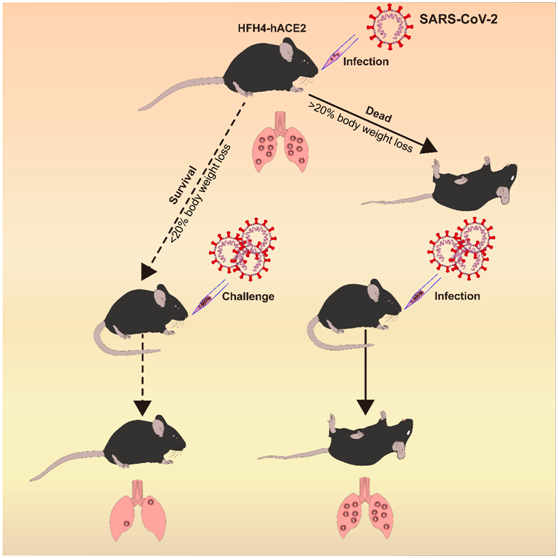
图2.HFH4-hACE2转基因小鼠模型模式图
《细胞》(Cell)期刊论文链接:
https://www.cell.com/cell/fulltext/S0092-8674(20)30622-X
 附件下载:
附件下载:
科学研究